3 磷酸可待因片藥典標準
3.1 品名
3.1.1 中文名
3.1.2 漢語拼音
Linsuan Kedaiyin Pian
3.1.3 英文名
Codeine Phosphate Tablets
3.2 含量或效價規定
本品含磷酸可待因(C18H21NO3·H3PO4·1.5H2O)應爲標示量的93.0%~107.0%。
3.3 性狀
本品爲白色片或包衣片。
3.4 鑑別
(1)在含量測定項下記錄的色譜圖中,供試品溶液主峯的保留時間應與對照品溶液主峯的保留時間一致。
(2)取本品的細粉適量,加水振搖後,濾過,濾液顯磷酸鹽的鑑別反應(2010年版藥典二部附錄Ⅲ)。
3.5 檢查
3.5.1 含量均勻度
取本品1片(15mg規格),置50ml量瓶中,加水適量,振搖1小時,使磷酸可待因溶解,用水稀釋至刻度,搖勻,濾過,取續濾液照含量測定項下的方法測定含量,應符合規定(2010年版藥典二部附錄Ⅹ E)。
3.5.2 溶出度
取本品,照溶出度測定法(2010年版藥典二部附錄Ⅹ
C第一法),以水900ml爲溶出介質,轉速爲每分鐘100轉,依法操作,經20分鐘時,取溶液10ml,濾過,精密量取續濾液適量,用水定量稀釋製成每1ml中約含磷酸可待因10μg的溶液,照紫外-可見分光光度法(2010年版藥典二部附錄Ⅳ A),在212nm的波長處測定吸光度,按C18H21NO3·H3PO4·1.5H2O的吸收係數(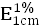 )爲601,計算每片的溶出量。限度爲標示量的80%,應符合規定。
)爲601,計算每片的溶出量。限度爲標示量的80%,應符合規定。
3.5.3 其他
應符合片劑項下有關的各項規定(2010年版藥典二部附錄Ⅰ A)。
3.6 含量測定
照高效液相色譜法(2010年版藥典二部附錄Ⅴ D)測定。
3.6.1 色譜條件與系統適用性試驗
用十八烷基硅烷鍵合硅膠爲填充劑,以0.03mol/L醋酸鈉溶液(用冰醋酸調節pH值至3.5)-甲醇(25:10)爲流動相;檢測波長爲280nm;理論板數按磷酸可待因峯計算不低於2000,磷酸可待因峯與相鄰雜質峯的分離度應符合要求。
3.6.2 測定法
取本品20片,精密稱定,研細,精密稱取適量(約相當於磷酸可待因30mg),置100ml量瓶中,加水溶解並稀釋至刻度,搖勻,濾過;精密量取續濾液10μl注入液相色譜儀,記錄色譜圖;另取磷酸可待因對照品適量,精密稱定,加水溶解並定量稀釋成每1ml中含0.3mg的溶液,同法測定。按外標法以峯面積計算,並將結果乘以1.068,即得。
3.7 類別
3.8 規格
(1)15mg (2)30mg
3.9 貯藏
3.10 版本
《中華人民共和國藥典》2010年版