3 国家基本药物
| 序号 | 基本药物目录序号 | 药品名称 | 剂型 | 规格 | 单位 | 零售指导价格 | 类别 | 备注 |
| 203 | 18 | 诺氟沙星 | 胶囊 | 100mg*20 | 盒(瓶) | 3元 | 化学药品和生物制品部分 | * |
| 204 | 18 | 诺氟沙星 | 胶囊 | 100mg*6 | 盒(瓶) | 0.94元 | 化学药品和生物制品部分 | |
| 205 | 18 | 诺氟沙星 | 胶囊 | 100mg*10 | 盒(瓶) | 1.5元 | 化学药品和生物制品部分 | |
| 206 | 18 | 诺氟沙星 | 胶囊 | 100mg*12 | 盒(瓶) | 1.8元 | 化学药品和生物制品部分 | |
| 207 | 18 | 诺氟沙星 | 胶囊 | 100mg*24 | 盒(瓶) | 3.6元 | 化学药品和生物制品部分 | |
| 208 | 18 | 诺氟沙星 | 胶囊 | 100mg*30 | 盒(瓶) | 4.4元 | 化学药品和生物制品部分 | |
| 209 | 18 | 诺氟沙星 | 胶囊 | 100mg*40 | 盒(瓶) | 5.9元 | 化学药品和生物制品部分 | |
| 210 | 18 | 诺氟沙星 | 胶囊 | 100mg*48 | 盒(瓶) | 7元 | 化学药品和生物制品部分 | |
| 211 | 18 | 诺氟沙星 | 胶囊 | 100mg*50 | 盒(瓶) | 7.3元 | 化学药品和生物制品部分 | |
| 212 | 18 | 诺氟沙星 | 胶囊 | 100mg*60 | 盒(瓶) | 8.6元 | 化学药品和生物制品部分 | |
| 213 | 18 | 诺氟沙星 | 胶囊 | 100mg*100 | 盒(瓶) | 14.1元 | 化学药品和生物制品部分 | |
| 214 | 18 | 诺氟沙星 | 片剂 | 100mg*10 | 盒(瓶) | 1.3元 | 化学药品和生物制品部分 | |
| 215 | 18 | 诺氟沙星 | 片剂 | 100mg*24 | 盒(瓶) | 3.1元 | 化学药品和生物制品部分 |
注(化学药品和生物制品部分):
1、表中备注栏标注“*”的为代表品。
2、表中代表剂型规格在备注栏中加注“△”的,该代表剂型规格及与其有明确差比价关系的相关规格的价格为临时价格。
注(中成药部分):
2、表中备注栏加注“△”的剂型规格,及同剂型的其他规格为临时价格。
4 诺氟沙星药典标准
4.1 品名
4.1.1 中文名
4.1.2 汉语拼音
Nuofushaxing
4.1.3 英文名
Norfloxacin
4.2 结构式
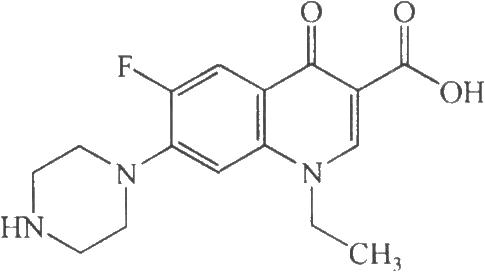
4.3 分子式与分子量
C16H18FN3O3 319.24
4.4 来源(名称)、含量(效价)
本品为1-乙基-6-氟-1,4-二氢-4-氧代-7-(1-哌嗪基)-3-喹啉羧酸。按干燥品计算,含C16H18FN3O3应为98.5%~102.0%。
4.5 性状
本品为类白色至淡黄色结晶性粉末;无臭,味微苦;有引湿性。
本品在二甲基甲酰胺中略溶,在水或乙醇中极微溶解;在醋酸、盐酸或氢氧化钠溶液中易溶。
4.5.1 熔点
本品的熔点为218~224℃(2010年版药典二部附录Ⅵ C)。
4.6 鉴别
(1)取本品与诺氟沙星对照品适量,分别加三氯甲烷-甲醇(1:1)制成每1ml中含2.5mg的溶液,作为供试品溶液与对照品溶液,照薄层色谱法(2010年版药典二部附录Ⅴ B)试验,吸取上述两种溶液各10μl,分别点于同一硅胶G薄层板上,以三氯甲烷-甲醇-浓氨溶液(15:10:3)为展开剂,展开,晾干,置紫外光灯(365nm)下检视。供试品溶液所显主斑点的位置与荧光应与对照品溶液主斑点的位置与荧光相同。
(2)在含量测定项下记录的色谱图中,供试品溶液主峰的保留时间应与对照品溶液主峰的保留时间一致。
以上(1)、(2)两项可选做一项。
4.7 检查
4.7.1 溶液的澄清度
取本品5份,各0.5g,分别加氢氧化钠试液10ml溶解后,溶液应澄清;如显浑浊,与2号浊度标准液(2010年版药典二部附录Ⅸ B)比较,均不得更浓。
4.7.2 有关物质
取本品适量,精密称定,加0.1mol/L盐酸溶液适量(每12.5mg诺氟沙星加0.1mol/L盐酸溶液1ml)使溶解,用流动相A定量稀释制成每1ml中约含0.15mg的溶液,作为供试品溶液;精密量取适量,用流动相A定量稀释制成每1ml中含0.75μg的溶液,作为对照溶液。另精密称取杂质A对照品约15mg,置200ml量瓶中,加乙腈溶解并稀释至刻度,摇匀,精密量取适量,用流动相A定量稀释制成每1ml中约含0.3μg的溶液,作为杂质A对照品溶液。照高效液相色谱法(2010年版药典二部附录Ⅴ D)测定,用十八烷基硅烷键合硅胶为填充剂;以0.025mol/L磷酸溶液(用三乙胺调节pH值至3.0±0.1)-乙腈(87:13)为流动相A,乙腈为流动相B;按下表进行线性梯度洗脱。称取诺氟沙星对照品、环丙沙星对照品和依诺沙星对照品各适量,加0.1mol/L盐酸溶液适量使溶解,用流动相A稀释制成每1ml中含诺氟沙星0.15mg、环丙沙星和依诺沙星各3μg的混合溶液,取20μl注入液相色谱仪,以278nm为检测波长,记录色谱图,诺氟沙星峰的保留时间约为9分钟。诺氟沙星峰与环丙沙星峰和诺氟沙星峰与依诺沙星峰的分离度均应大于2.0。取对照溶液20μl注入液相色谱仪,以278nm为检测波长,调节检测灵敏度,使主成分色谱峰的峰高约为满量程的25%。精密量取供试品溶液、对照溶液和杂质A对照品溶液各20μl,分别注入液相色谱仪,以278nm和262nm为检测波长,记录色谱图。供试品溶液色谱图中如有杂质峰,杂质A(262nm检测)按外标法以峰面积计算,不得过0.2%。其他单个杂质(278nm检测)峰面积不得大于对照溶液主峰面积(0.5%);其他各杂质峰面积的和(278nm检测)不得大于对照溶液主峰面积的2倍(1.0%)。供试品溶液色谱图中任何小于对照溶液主峰面积0.1倍的峰可忽略不计。
| 时间(分钟) | 流动相A(%) | 流动相B(%) |
| 0 | 100 | 0 |
| 10 | 100 | 0 |
| 20 | 50 | 50 |
| 30 | 50 | 50 |
| 32 | 100 | 0 |
| 42 | 100 | 0 |
4.7.3 干燥失重
取本品,在105℃干燥至恒重,减失重量不得过1.0%(2010年版药典二部附录Ⅷ L)。
4.7.4 炽灼残渣
取本品1.0g,置铂坩埚中,依法检查(2010年版药典二部附录Ⅷ N),遗留残渣不得过0.1%。
4.7.5 重金属
取炽灼残渣项下遗留的残渣,依法检查(2010年版药典二部附录Ⅷ H第二法),含重金属不得过百万分之十五。
4.8 含量测定
照高效液相色谱法(2010年版药典二部附录Ⅴ D)测定。
4.8.1 色谱条件与系统适用性试验
用十八烷基硅烷键合硅胶为填充剂;以0.025mol/L磷酸溶液(用三乙胺调节pH值至3.0±0.1)-乙腈(87:13)为流动相,检测波长为278nm。称取诺氟沙星对照品、环丙沙星对照品和依诺沙星对照品各适量,加0.1mol/L盐酸溶液适量使溶解,用流动相稀释制成每1ml中含诺氟沙星25μg、环丙沙星和依诺沙星各5μg的混合溶液,取20μl注入液相色谱仪,记录色谱图,诺氟沙星峰的保留时间约为9分钟。诺氟沙星峰与环丙沙星峰和诺氟沙星峰与依诺沙星峰的分离度均应大于2.0。
4.8.2 测定法
取本品约25mg,精密称定,置100ml量瓶中,加0.1mol/L盐酸溶液2ml使溶解后,用水稀释至刻度,摇匀,精密量取5ml,置50ml量瓶中,用流动相稀释至刻度,摇匀,精密量取20μl注入液相色谱仪,记录色谱图;另取诺氟沙星对照品,同法测定,按外标法以峰面积计算,即得。
4.9 类别
喹诺酮类抗菌药。
4.10 贮藏
4.11 制剂
(1)诺氟沙星软膏 (2)诺氟沙星乳膏 (3)诺氟沙星胶囊 (4)诺氟沙星滴眼液
4.12 附:
杂质A:1-乙基-6-氟-7-氯-4-氧代-1,4-二氢喹啉-3-羧酸
4.13 版本
《中华人民共和国药典》2010年版
5 诺氟沙星介绍
5.1 别名
力醇罗片;淋克小星;诺氟沙星 ;力醇罗;氟哌酸; 淋沙星;淋克星。
5.2 外文名
Norfloxacin, AM-715, Brazan, Fulgram, Lexnor, MK-0366, Uroxacin, Noroxin, Zoroxin
5.3 诺氟沙星的适应症
用于泌尿道、呼吸系统、肠道、耳鼻喉科、妇科、外科和皮肤科等感染性疾病。
5.4 诺氟沙星的用量用法
口服:成人一般用量为每日400mg~800mg,分为3~4次服,伤寒或其他沙门氏菌感染用每日800~1600mg,分4次服。空腹服药吸收较好。一般疗程为3~8日,少数病例可达3周。对于慢性泌尿道感染病例,可先用一般量2周,再减量为每日200mg,睡前服用,持续数月。
5.5 注意事项
1.服药初期可有上腹部不适感,一般无需停药,可逐渐自行消退,但有胃疡史的病人应慎用。
2.少数病人可引起转氨酶升高,停药后可恢复正常。
3.少数病人可出现周围神经刺激症状,四肢皮肤有针刺感,或有轻微的灼热感,加用维生素B1和B12可减轻。
5.6 规格
胶囊:每胶囊100mg、200mg。 水针剂:0.2g(100ml),0.1g(100ml)。