3 概述
絕經後骨質疏鬆症(postmenopausal osteoporosis,POP)是一種與衰老有關的常見病,主要發生在絕經後婦女,由於雌激素缺乏導致骨量減少及骨組織結構變化,使骨脆性增多易於骨折,以及由骨折引起的疼痛、骨骼變形、出現合併症,乃至死亡等問題,嚴重地影響老年人的身體健康及生活質量,甚至縮短壽命,增加國家及家庭財力與人力負擔。與絕經相關的骨質疏鬆症已是不可忽視的重要保健課題。1993年WHO對骨質疏鬆症定義爲是全身性的骨量減少,伴隨骨的微結構改變,導致骨脆性增加,因而骨折危險性增加的一種疾病。2001年美國國立衛生院共識會議提出,骨質疏鬆症是以骨強度受損爲特徵的骨骼疾病,導致骨折危險性增加。骨強度集中反映骨密度與骨質量。骨質疏鬆症的病理特點是骨礦含量和骨基質成分等比例地減少,骨皮質變薄,骨小梁減少、變細,絕經後骨質疏鬆症時骨小梁斷裂。
9 流行病學
世界人口統計學顯示,60歲以上的人口比例正快速增加,許多國家婦女的平均壽命已達70歲或80歲,由於多數婦女的絕經年齡爲45~55歲,因而絕經後婦女人數增加。
但骨質疏鬆症及骨質疏鬆性骨折發生率有很大差異,歐洲各國相差達10倍之多,但以下觀點是一致的:
1.婦女發生骨質疏鬆症及其相關的骨折率均顯著高於男性,例如美國白人婦女一生中患髖部骨折的危險性是17%,而男性是6%。澳大利亞60歲以上婦女發生骨質疏鬆症的危險性爲58%,男性爲28%;英國45歲以上發生的骨折中,85%爲女性,而且不包括脊椎骨折。Kanis提出,女性骨質疏鬆性骨折的危險性是男性的3倍,西方婦女在50歲時骨質疏鬆性骨折的終身危險大約爲40%,相當於婦女患心血管病的危險性,高於乳癌(9%)。女性發病率高的主要原因是骨峯值低於男性(約25%),同時又有絕經後骨丟失加速的影響,例如婦女在絕經後5~10年內,每年骨丟失率爲5%(2%~10%),而男性平均爲1%。此外,男性的骨丟失是骨小梁變細,而不是斷裂,因此女性的骨脆性較男性高,易於發生骨折。
2.黑人的骨密度較白人高,骨質疏鬆症發病率顯著低於白種人,亞洲人與白種人相近。
3.髖部骨折是骨質疏鬆症的最嚴重合並症。日本於1987年共發生股骨頸骨折5萬例,1992年上升至8萬例。我國解放軍總醫院對北京市1400例絕經後婦女測定腰椎,按WHO 1994年修訂的骨質疏鬆症診斷標準,發生率爲17%。北京協和醫院調查北京城區50歲以上女性髖部骨折的發生率爲88/10萬。
10 絕經後骨質疏鬆的病因
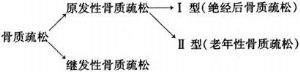
Ⅰ型骨質疏鬆又稱爲絕經後骨質疏鬆,主要原因是雌激素缺乏,發生於女性患者,年齡在50~70歲,表現出骨量迅速流失,骨松質丟失更明顯,骨折多發生在以骨松質爲主的椎體,股骨上端及橈骨遠端。
Ⅱ型骨質疏鬆又稱老年性骨質疏鬆。與Ⅰ型比較,男性患者增加,但男女之比仍爲1:2,發病年齡多在70歲以上,表現爲骨量緩慢丟失,骨松質與骨密質丟失速度大致相同,骨折好發部位除與Ⅰ型相同外,髖部骨折的發生率有所增加。
1983年,Riggs對Ⅰ、Ⅱ型骨質疏鬆症進行比較(表1)。

繼發性骨質疏鬆是由其他病因引起的。如慢性疾病:慢性腎功能衰竭、胃切除、腸改道、鈣吸收不良綜合徵、多發性骨髓瘤等;內分泌疾病:高泌乳素血癥、甲狀腺功能亢進、腎上腺皮質激素分泌過多、糖尿病、甲狀旁腺功能亢進等。醫源性因素:長期應用抗癲癇藥、含鋁抗酸劑、服用過量甲狀腺素或長期應用糖皮質激素、促性腺激素釋放激素(GnRH)激動劑等。
絕經後骨質疏鬆是多因素性疾病,遺傳、生活方式、營養等均與發病有關。具有以下高危因素者易患絕經後骨質疏鬆症:白人及亞洲婦女、骨質疏鬆症家族史、或具有影響骨量的特殊基因的婦女、鈣攝入不足、缺乏體力活動、大量吸菸及飲酒、早絕經或絕經前行雙側卵巢切除術者。是否發生骨質疏鬆症,取決於其骨峯值及其骨丟失的速度,骨峯值高及(或)骨丟失慢者,不易發生,骨峯值低及(或)骨丟失快者容易發生。
10.1 骨峯值
骨峯值指個人一生中的最高骨量,一般在25~35歲時達到。影響骨峯值的因素很多,其中遺傳因素最爲重要,營養、生活習慣等也有一些影響。
10.1.1 (1)遺傳因素
決定骨峯值的70%~80%。例如黑人BMD高於白人及亞洲人,其骨質疏鬆性骨折發生率低,骨質疏鬆有家族傾向、單卵雙胎的BMD差異較雙卵雙胎者小、男性的骨峯值高於女性、在有些國家,維生素D受體基因、雌激素受體基因、或膠原基因的多態性與BMD有關等,均證明骨峯值受遺傳因素影響。
10.1.2 (2)營養
青春期內鈣攝入量高者,骨峯值較高,對成熟骨BMC的影響可達6%。世界衛生組織推薦,青春期內元素鈣攝入量應爲每天1000mg。
10.1.3 (3)生活習慣
運動可增加BMD,如果堅持每天鍛鍊,其體力活動量高於平均量1SD時,其骨量較活動量低於平均量1SD者高7%~10%。但運動過度引起性腺功能低下而發生閉經時,骨量反而降低。骨峯值形成前大量吸菸、嗜酒者骨峯值低。
10.1.4 (4)原發性性腺功能不足及青春期發育延遲者,骨峯值低。
10.2 骨丟失率
婦女的骨丟失與增齡及絕經有關。
10.2.1 (1)與年齡相關的骨丟失
脊椎骨丟失一般自40~50歲開始,丟失率爲每年0.8%~1.2%。四肢骨的丟失大約晚10年,即自50~60歲開始,丟失率爲每年0.3%~0.6%,均呈線性,其發生機制不清楚,可能與骨形成減少有關。這種骨丟失的後果是骨小梁變細,不發生骨小梁的穿孔性變化。
10.2.2 (2)與絕經相關的骨丟失
不論年齡,婦女一旦絕經,體內的雌激素即急劇下降,骨丟失呈對數增加,骨小梁變細、變薄、乃至斷裂(穿孔)。雙側卵巢切除術後,卵巢來源的性激素全部消失,骨丟失速度更快,此時脊椎骨丟失是四肢骨的兩倍,丟失率高達每年4%~5%,持續5~10年後,骨丟失速度才減慢。四肢骨的骨丟失慢,丟失的持續時間也長。
動物試驗及臨牀觀察證實,去卵巢動物或絕經後婦女補充雌激素後,骨轉換率降低,可以有效地防止骨丟失,由此也證明,雌激素不足是絕經後骨質疏鬆症的主要發病原因。
11 發病機制
正常骨骼通過骨重建使骨質不斷地得到更新。破骨細胞的溶骨作用在骨表面下挖空形成骨陷窩,隨後由一羣成骨細胞向骨陷窩移行,合成和分泌膠原以及與骨形成有關的多肽蛋白。鈣離子沉積後形成骨基質,骨陷窩由新形成的骨基質得到修補,完成一個骨重建單位,週期大約爲3~4個月。骨轉換率是指舊骨吸收和新骨形成過程的速率,絕經後雌激素降低,骨轉換增加,骨丟失增加,呈現高轉換型骨質疏鬆。雌激素對骨質疏鬆發病的影響,主要是通過以下途經實現。
11.1 對鈣調節激素的作用
雌激素可以增強肝25-羥化酶、腎1α-羥化酶活性,提高1,25-雙羥維生素D水平,促進腸鈣吸收,並使鈣鹽和磷鹽在骨質中沉積,促進骨基質合成。雌激素還有拮抗甲狀旁腺素的作用,與甲狀旁腺素共同維持血中鈣磷平衡。甲狀旁腺素是刺激骨溶解的激素,當雌激素減少,對甲狀旁腺素拮抗作用減弱,可以加速骨質消融而逐漸發展爲骨質疏鬆。降鈣素具有抑制破骨細胞活性,雌激素可促進降鈣素分泌。
11.2 通過細胞因子的作用參與骨形成與吸收過程
自從1988年Komm證明成骨細胞中有雌激素受體存在之後,Ernst發現外源性雌激素可促進大鼠成骨細胞產生IGF-I。由於IGF-I的產生增強,使雌激素受體過度表達。還發現雌激素能促進成骨細胞中TGF-β的產生,表明這些生長因子對骨形成有促進作用,雌激素通過這些生長因子的產生,促進骨形成。
實驗表明,當雌激素缺乏,骨髓單核細胞分泌IL-1和間質細胞分泌IL-6都增多。Pacifici等還發現在培養的末梢血單核細胞中能產生TNF-α和GM-CSF;切除卵巢的患者體內TNF-α和GM-CSF水平升高,接受雌激素治療的患者TNF-α和GM-CSF恢復到正常水平。以上細胞因子對骨吸收過程有促進作用,雌激素通過抑制上述細胞因子的產生而抑制骨吸收(圖1,2)。
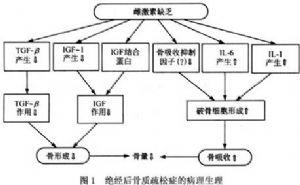

11.3 雌激素對骨細胞的直接作用
自從1988年komm在成骨細胞上發現了雌激素受體(ER),1990年Penlser又在破骨細胞上發現了雌激素受體,更加明確了雌激素與骨細胞的直接作用關係。雌激素可與成骨細胞和破骨細胞上的雌激素受體結合,直接抑制破骨細胞的溶酶體酶活性,降低其在骨切片上產生陷窩的能力。1996年Shevde在去勢大鼠模型上證明雌激素可通過受體結合途徑,直接抑制破骨細胞前體形成細胞(骨髓造血幹細胞)的募集、分化,從而抑制破骨細胞活性,且利用細胞形態學方法證明,雌激素的這種作用是通過影響細胞週期誘導細胞凋亡來實現的。1997年kameda應用高度純化的哺乳動物成熟的破骨細胞,也得出了相似的結論。Ernst證實雌激素增強了大鼠原始顱骨細胞的繁殖及細胞內膠原、IGF-I mRNA的表達。
12 絕經後骨質疏鬆的臨牀表現
骨質疏鬆症是一種隱匿發生的疾病,在沒有發生骨折之前,往往沒有任何症狀,一旦發現駝背、身材變矮、或骨痛時,常常已經發生了骨折。因此,不能用臨牀症狀進行診斷,疼痛的嚴重程度可用於判斷治療效果。
12.1 骨痛
骨質疏鬆的骨痛,通常是因小梁骨發生微骨折,當體位變動時肌肉及韌帶牽拉引起,故可發生起坐痛、前屈後伸痛、行走痛、翻身痛及臥位痛等。通常用四級評分法反應疼痛程度,0分爲無痛,1分爲有時疼痛,2分爲經常疼痛,但能忍受,3分爲疼痛難忍,並影響工作及生活。
12.2 駝背或身材變矮
12.3 局部壓痛或叩擊痛
局部壓痛或叩擊痛的特點是不伴隨局部紅腫及發熱。
13 絕經後骨質疏鬆的併發症
13.1 骨折
骨折是骨質疏鬆所致的最主要的併發症,如因骨折而臥牀不起,則易導致肺炎,心血管疾病等併發病常發生脊椎、前臂及髖部骨折。與健康人發生骨折的區別是輕微外傷即發生骨折。
13.1.1 (1)脊椎骨折
提舉或推拉重物,彎腰,輕微跌倒,或跌倒時臀部着地時即可發生脊椎壓縮性骨折,出現急性及嚴重的腰、背疼痛,有時伴隨身材變矮,或有神經根壓迫性疼痛。如果脊椎壓縮性骨折逐漸發生,則出現慢性腰背痛。
13.1.2 (2)前臂骨折
13.1.3 (3)髖部骨折
輕微滑倒即可發生髖部骨折,常見於年齡較大的絕經後婦女。因髖部骨折發生後,15%~30%在1年內死於各種合併症,存活者中,約半數生活不能自理,因而是骨質疏鬆症的最嚴重的合併症。
13.2 胸悶、氣急、咳嗽、腹脹、便祕等症狀
14 實驗室檢查
14.1 骨吸收生化指標
14.1.1 (1)尿Ca/Cr
骨吸收時骨鈣進入血循環,引起血鈣升高,爾後尿鈣升高,故尿鈣可以反映骨吸收狀況。飲食中的鈣含量、腸鈣吸收及腎功能情況等影響血及尿鈣水平,故特異性不強。空腹12h後的尿鈣可避免食物的影響,主要反應骨吸收狀況,爲避免前日飲食的影響,空腹12h後的第一次尿棄去,留取空腹的第二次尿測定。
14.1.2 (2)尿HOP/Cr
尿HOP的50%爲骨膠原的代謝產物,骨吸收增加時,比值升高。爲避免飲食的影響,除需留取空腹的第二次尿之外,應在留尿標本的前3天禁食含膠原多的食物。
14.1.3 (3)Ⅰ型膠原吡啶交聯物及末端肽
Ⅰ型膠原吡啶交聯物及末端肽是骨、軟骨及其他結締組織中膠原的代謝產物,骨吸收增加時,血或尿中的含量增多,因爲骨組織的轉化率遠高於軟骨及結締組織,故主要反應骨的吸收狀況,其水平不受飲食影響,較尿Ca/Cr及尿HOP/Cr反映骨吸收的特異性強。目前多測定尿Pyr/Cr、DPYr/Cr;血的Ⅰ型膠原交聯氨基末端肽(NTx)或c-端多肽(CTx)。NTx是破骨細胞降解膠原的直接產物,而CTx的結構爲所有組織中的Ⅰ型膠原所共有,故其特異性較NTx差。
14.1.4 (4)血抗酒石酸酸性磷酸酶(TRAP)
TRAP由破骨細胞合成並直接分泌入血,因而反映破骨細胞的狀況,骨吸收增加時,血TRAP升高。
14.2 骨形成生化指標
14.2.1 (1)血清鹼性磷酸酶(ALP)及骨鹼性磷酸酶(bALP)
ALP由肝及成骨細胞產生,小腸來源者佔25%,空腹時比例減少,腎來源者很少,可以不計,故在肝功能正常時,它反映成骨細胞的活性。bALP只來源於成骨細胞,故特異性強。
14.2.2 (2)血清骨鈣素(BGP)
BGP是骨組織中最豐富的非膠原蛋白,由成骨細產生,成熟的BGP分子分泌到細胞外,其中大部分進入細胞外骨基質,小部分進入血循環。絕經後骨質疏後骨質疏鬆婦女血中的BGP可能升高、降低或正常,取決於其骨形成速率。骨形成刺激劑治療後BGP水平升高,而使用骨吸收抑制劑後,BGP水平降低。腎功能不良者,血BGP升高(BGF由腎濾過及降解)。
14.2.3 (3)血清I型膠原前肽
I型膠原由成骨細胞合成,其氨基端(N-端,PINP)和羧基端(C-端,PICP)延長肽被特異酶切下後,可以測定,反映膠原的合成狀況。然而皮膚、牙齒、心血管等能合成I型膠原的組織也可產生。
15 輔助檢查
15.1 骨礦含量(BMD)測定
BMD目前是診斷骨質疏鬆的主要依據,因爲骨密度在很大程度上可以預測骨折的危險性,WHO於1994年修訂骨量測定值的診斷標準爲BMD或BMC較正常成年人平均值低2.5s以上,稱爲T-分(T-Score),其計算方法爲(測定的BMD-正常成年人平均BMD)÷標準差。但骨折的發生不僅僅取決於BMD,而是與骨強度有關,骨強度由BMD與骨質量組成,因此,診斷方法還有待完善。
15.1.1 (1)BMD的測定方法
15.1.1.1 ①X線照片
X線照片是最早應用的定性或半定量的骨量測定法。所謂定性,是用肉眼觀察骨組織與其旁的軟組織之間的密度差,差別大者骨密度高,差別小者骨密度低,無差異者骨密度最低。此外,骨紋粗而密集者骨密度高,骨紋細而稀疏者骨密度低;骨皮質厚者骨密度高,反之則低。嚴重的骨質疏鬆症時,骨紋細少且伴隨皮質骨呈線狀。1955年Lachman提出BMD丟失30%~50%才能在X線照片上發現,故不能用於早期診斷。後來出現了半定量的方法,即股骨頸小梁指數法(Singh指數)及跟骨小梁指數法等。股骨頸小梁指數法是根據股骨頸骨小梁的分佈多少分爲Ⅰ-Ⅶ級,Ⅲ級以下者,肯定爲骨質疏鬆。跟骨小梁指數法是根據骨小梁密度分爲5度,5度及4度者爲正常,3度可疑,1度及2度爲骨質疏鬆。
目前X線照片在骨質疏鬆症中的應用價值,在於診斷是否合併骨折,是否伴有骨質增生及骨骼變形,並與其他骨病鑑別,如骨腫瘤,骨軟化症等,因此,並不能廢棄。
15.1.1.2 ②單能光子吸收儀(SPA)
SPA是20世紀60年代發展的骨量測定技術,其原理是放射性核素產生的射線透過人體時,可被骨組織吸收,未被吸收的部分由放射源對側的探測器接收,射線計數經電腦自動處理,以數字顯示骨礦含量(BMC)、骨寬度(BW)及BMD(BMC/BW)。BMC以g/cm表示,BW以cm表示,BMD則爲g/cm2。骨量高時,探測器接收的射線量低,反之則高。
核素用125碘(125I)或241鎇(241Am)。125I的半衰期爲60天,需定期更換,241Am的半衰期爲433年,可長期使用。此法適用於測定肌肉少的四肢骨,不能測定深部骨骼,如脊椎骨及股骨。前臂骨形態規律,骨周圍爲均一性薄層軟組織,而且骨與軟組織的比例高,測定中不易受技術因素的影響,故多用於前臂骨的測定。其精確度爲1%~2%,準確度爲4%~6%,一次測定需5~10min,放射量小於1/µSV。因價格較低、適用於普查,但前臂中、外1/3交界處的皮質骨較多,絕經後變化較小,而測量前臂遠端,雖松質骨較多,但因接近關節,骨形態不規則,測定值不甚理想,是其主要缺點。
測定方法:將前臂浸泡於水槽內,或包一水囊(使其吸收的光子相等於軟組織,那麼,對放射線的吸收差異只由骨組織構成)。選定測量部位,機器即自動在肢體上移動探測器,並自動顯示測定值。
15.1.1.3 ③雙能光子吸收儀(DPA)
DPA與SPA的區別是應用兩個能量不同的放射源,將兩種能量的計數經處理後相減,則消除全部軟組織的計數,剩下的就是骨組織的計數。故可測量脊椎骨及股骨等深部骨骼,但因其測量的精確度及準確度較差,檢查時間長,於20世紀80年代末已被DXA取代。
15.1.1.4 ④雙能X線吸收儀(DXA)
DXA原理與DPA相同,但放射源不用核素,而是利用X線管。用濾光板將X線球管產生的光子束分爲兩種能量的X線,故能消除骨組織周圍肌肉厚薄不同的影響,可測量脊椎骨,髖部及全身任何部位骨骼的BMC及BMD,並可測量肌肉及脂肪含量。用筆形X線束掃描時間需6~15min,用扇形X線束掃描只需2min。精確度爲1%~2%,準確度爲4%~8%,放射劑量爲1µSV。目前認爲是診斷骨質疏鬆症及判斷療效的可靠方法。
測定方法:被測者平臥於機器上,測定脊椎骨時,可經前後位或側位測定。前後位測定的缺點是老年病人易受骨質增生及主動脈硬化的影響而出現假陰性(測定值比實際高)。測定髖部時,一般測定股骨頸、Wards三角區及大粗隆,故需內旋股骨45°,使測定部位顯露清楚。
⑤單能X線吸收儀(SXA):與SPA的用途及原理相同,不同之處是放射源用X線,而不用核素。北京協和醫院用SXA測定前臂與DXA測定腰椎、股骨頸、Wards區、大粗隆相比,兩種方法的相關性良好。
15.1.1.5 ⑥定量計算機斷層攝影(QCT)
QCT是目前惟一可以在三維空間測量BMD而得出真實體積BMD的方法,測定值爲g/cm3,也是目前可以分別測量皮質骨與松質骨BMD的惟一方法,用於測量腰椎BMD。測量時將標準體模置於病人的背部,與病人同步掃描,掃描時間爲10~20min,精確度爲2%~5%,準確度爲3%~6%,放射劑量約爲100µSV。因放射劑量較大,不宜多次重複檢查。
用於測量四肢的QCT爲pQCT,其精確度提高到0.5%~1%,放射劑量也大大減少。日本婦女中用pQCT測量橈骨BMD與DXA測量脊椎、橈骨及股骨頸BMD相比,有中度相關,預測骨折的可靠性次於DXA。故能否用於診斷尚有爭議。
15.1.2 (2)BMD測定的質控指標
精確度指重複測量一個部位的變異,亦稱重複誤差,或精確度誤差。通常以變異係數(CV)表示,CV越大,精確度越差。CV計算法爲:
CV=(標準差/BMD均值)×100%
精確度的臨牀意義在於:判斷療效時,如精確度爲1%,取95%可信限時,BMD變化大於±2.8%纔有意義,否則爲儀器本身的誤差,不能判斷有效或無效。取90%可信限,BMD變化在±2%即有臨牀意義。如果骨丟失率爲每年3%,用精度爲1%的儀器可以測量出變化,而精度差(即大於1%)的儀器則測不出來。設計臨牀療效觀察應人組的例數,例如精度爲1%時,發現BMD增加0.5%,需要42人(按統計學公式)。
準確度:指測量值與真值(如骨灰量)之間的誤差,即儀器的誤差,由廠家提供。誤差大者易出現假陽性,小於真值則出現假陰性。
15.2 骨超聲檢查
利用超聲通過骨組織的速度(SOS,單位爲m/s)、振幅衰減(BUA,單位爲dB/MHz)及硬度指數(SI)反映骨結構與骨量,在理論上,超聲檢查既反映骨量又反映骨結構,且具有無放射線,價格較低,機器易搬動等許多優點,有人將超聲檢查值與DXA檢查結果相比,二者有相關性,故可用於觀察病情變化及治療效果。但超聲檢查結果不是BMC,故不能與真值相比,無準確性指標,目前尚無公認的診斷標準。
15.3 骨組織活體切片檢查
將活體骨組織製成切片,在顯微鏡下觀察結構與形態,測量骨小梁面積、骨小梁周徑、類骨質寬度等骨形態計量學指標,可用於疑難病例的鑑別診斷,研究骨代謝狀況。與上述的幾種方法相比,診斷更爲可靠,但是觀察結果有一定的主觀性,故各實驗室間、各觀察者之間有一定的差異,此外,骨活檢是有創性檢查,不宜普遍進行。
16 絕經後骨質疏鬆的診斷
根據以上臨牀表現,實驗室檢查及輔助檢查可以在骨質疏鬆早期即做出診斷。
骨礦含量是診斷骨質疏鬆的標準1994年WHO重新制訂了以骨密度作爲骨質疏鬆的診斷標準:
1.正常骨量:BMD或BMC較年輕成年人平均值低1個標準差以內。
2.骨量減少:BMD或BMC較年輕成年人平均值低1~2.5個標準差。
3.骨質疏鬆症:BMD或BMC較年輕成年人平均低2.5個標準差或以上。
4.嚴重的骨質疏鬆症(確定的骨質疏鬆症):符合上述的骨質疏鬆症診斷標準。同時伴有一處或多處脆性骨折。
我國專家認爲以骨量丟失平均值的2.5個標準差不利於骨質疏鬆症的早期診斷和治療,以丟失2個標準差爲診斷標準更適合我國國情。
17 鑑別診斷
17.1 多發性骨髓瘤
多發性骨髓瘤與骨質疏鬆相似之處爲骨量降低,骨痛及病理性骨折。不同之處是多發性骨髓瘤在X線照片上有骨破壞區,病情呈進行性加重,病變多見於頭顱和骨盆,骨髓穿刺檢查有助於確診。
17.2 骨轉移瘤
骨轉移瘤常見於老年婦女,患者可伴有骨痛,骨量減少及(或)病理性骨折。與骨質疏鬆症的主要區別是可能發現原發腫瘤,X線照片上有骨破壞區。
17.3 骨軟化症
因骨軟化症時BMD也降低而需與骨質疏鬆症鑑別,但骨軟化症常發生於生育期婦女,其發病與多產及營養不良有關,常有手足抽搐,血鈣及血磷降低,血tALP升高等改變,骨X線照片可見骨邊界有絨毛狀變化,而絕經後骨質疏鬆症發生於絕經後婦女,通常無症狀,血鈣、磷正常,血tALP在正常範圍內升高,骨X線照片上骨邊界清晰。但高齡婦女缺乏戶外活動,維生素D攝入不足,可能同時患有骨質疏鬆及骨軟化症。
17.4 繼發性骨質疏鬆症
繼發性骨質疏鬆症是由各種疾病或長期應用藥物引起的骨質疏鬆症,疾病如甲狀腺功能亢進症,甲狀腺功能減低,甲狀旁腺功能亢進,糖尿病,庫欣綜合徵,慢性肝病,腎病,嚴重的營養不良等,藥物如腎上腺皮質激素,甲狀腺激素,促性腺激素釋放激素類似物(GnRH-α),肝素,化療藥物等。可發生於任何年齡,詳細詢問病史及體格檢查,輔以必要的實驗室檢查,即可與絕經後骨質疏鬆症鑑別。
18 絕經後骨質疏鬆的治療
18.1 激素替代療法(HRT)
已有大量研究證實絕經後婦女單獨應用雌激素或與孕激素聯合應用可以預防骨量的丟失。一項絕經婦女雌、孕激素干預36個月的研究,結果證實安慰劑組腰椎BMD下降1.8%,髖骨BMD下降1.7%;而雌激素組與雌、孕激素聯合治療組結合雌激素(倍美力CEEs)0.625mg/d組、結合雌激素(CEEs)+甲羥孕酮(安宮黃體酮MPA)2.5mg/d組、結合雌激素(CEEs)+甲羥孕酮(MPA)10mg/d組、結合雌激素(CEEs)+微粒化孕酮200mg/d×12天/月組,腰椎BMD增加3.5%~5.0%,髖骨BMD增加1.7%。另一項多中心研究納入9704名非黑人婦女,年齡≥65歲,目前應用雌激素者,與未用者相比,腕骨骨折危險性爲0.39(95%Cl 0.24~0.64),所有非脊椎骨折危險性爲O.66(95%Cl 0.54~0.80)。Deng等指出不同的維生素D受體與雌激素受體基因類型對骨密度影響不同。
雌激素的劑量與療效有明顯關係。不同種類藥物的最低有效劑量不同,如結合雌激素劑量爲0.625mg/d,雌二醇爲1mg/d,強調使用最低的有效劑量以避免其副作用。
George對絕經後雙胎婦女的研究發現目前使用HRT者其腰椎、髖骨骨密度比未用者增加,但以往使用HRT者無相似的有益作用。表明HRT需連續應用,如需停止,則應加用其他治療以保持對骨量的有利影響。
18.2 補鈣
適量鈣攝入對獲得骨峯量及保持骨髂健康是非常必要的。對絕經婦女推薦的每天鈣攝入量爲1000~1500mg元素鈣。我國居民的膳食結構處於低鈣飲食品狀態,1992年全國營養調查發現城市和農村成年男性平均每人每天鈣攝入量僅爲458mg和378mg:1994年的一項調查發現北京老年婦女每天鈣攝入量也低於400mg。改變飲食習慣,增加膳食中鈣的攝入,應多喫含鈣豐富的食物如牛奶、豆製品、海魚、蝦皮、紫菜及深綠色葉菜等,這是從食物中補鈣的有效措施之一。此外還可通過鈣製劑補充,如美信鈣,每片含檸檬酸鈣315mg,此外還含有維生素D,300IU,每天口服1片。樂力鈣含氨基酸螯合鈣及多種微量元素,每片含鈣量250mg,1粒/d。鈣爾奇D每片含碳酸鈣及維生素D 400U,鈣含量爲600mg,1粒/d。
對老年婦女較長時間的鈣劑補充可能部分逆轉與年齡相關的血清甲狀旁腺素(PTH)及骨吸收的增加,降低骨丟失。然而這種作用是較弱的,與雌激素、雙磷酸鹽、降鈣素比較,不能代替它們的治療作用,可作爲輔助治療,聯合應用。由於鈣劑的安全性,較高的耐受性及花費較低,每天鈣劑的補充是減少骨折危險的有效方式。儘管補鈣是相對安全的,仍應注意監測血、尿中鈣濃度,如果血鈣在正常範圍,24h尿鈣在100~200mg,說明劑量恰當;如果尿鈣在300~400mg,說明鈣或維生素D劑量過大,應減量;如果尿鈣>400mg,應停服以免出現腎或膀胱結石。
18.3 維生素D(vitamin D)
骨質疏鬆患者的負鈣平衡的原因之一是由於腸道鈣吸收障礙。影響腸道鈣吸收最重要的激素是1,25(0H)2D3,如含量少,即使食物中含鈣量較多,也難以吸收。維生素D在肝內經肝細胞線粒體的25-羥化酶(25-hydroxylase)作用,被羥化成25(OH)D3,轉運到腎臟,由1α-羥化酶或24-羥化酶等作用下再次被羥化成1,25(OH)2D3或24,25(0H)2D3等。其中1,25(0H)2D3是維生素D的活性代謝產物,也就是腎臟分泌的激素。1,25(OH)2D3對骨有直接作用,生理濃度的1,25(OH)2D3可同時促進骨吸收和骨形成。在成骨細胞中有1,25(OH)2D3受體,添加生理濃度的1,25(OH)2D3,可增加鹼性磷酸酶活性及膠原的產生。目前已確認1,25(0H)2D3除促進腸鈣吸收外,對骨組織的直接作用有骨石灰化、骨形成、骨成長作用及骨鹽類動員作用。
維生素D對鈣吸收及骨健康起了很重要的作用。食物中的維生素D包括含維生素D的牛奶(每夸脫含400U),麥片粥、蛋黃、海魚及魚肝油等。一些鈣劑及多種維生素片劑內也含有維生素D。Komulainen等認爲低劑量維生素D補充對於絕經後早期,非骨質疏鬆症婦女的預防作用較小,對使用HRT者沒有更顯著的效果。對老年婦女每天補充400U維生素D3可以輕度降低PTH的分泌,增加股骨頸骨密度,但骨轉換的生化指標未見變化。對維生素D缺乏的高危老年婦女,如慢性疾病、缺乏戶外活動、長期居家或者在養老院的老人建議每天補充400~800U維生素D。成年人通過紫外線皮膚照射和食物攝取,可以獲得足夠的維生素D。老年人由於肝臟25-羥化酶以及腎臟1α-羥化酶缺乏,宜選擇活性維生素D,如1α(OH)D3(阿法迪三),骨化三醇(1,25(0H)2D3,羅鈣全)等補充效果較好,劑量一般爲0.25~0.5µg/d,口服。
18.4 運動
絕經後有低骨量的婦女,骨丟失是緩慢的,可能通過運動加上鈣劑補充,或者加上HRT而得到預防。一些研究已發現運動加上雌激素比單用雌激素治療更爲有效,預防骨丟失需要的運動量及類型、方式尚不清楚。一項研究發現運動對絕經前後婦女可以預防或逆轉大約每年1%的腰椎及股骨頸的骨量丟失。另一項研究顯示體力活動對腰椎2~4水平的骨密度有顯著作用,然而未能發現對前臂及髖骨骨量的有效作用。
18.5 雙磷酸鹽
二磷酸鹽是20世紀50年代開發的強力骨吸收抑制劑,用於治療骨吸收加速的疾病,如變形性骨類(Pagets病)、惡性腫瘤骨轉移及其伴隨的高鈣血癥等;當骨轉換加快時,效果最好,因而也適用於絕經後骨質疏鬆症。雙磷酸鹽與體內的鈣代謝調節劑——焦磷酸鹽結構相似,對羥磷灰石親和力強,與之結合後集聚在骨內,抑制磷酸鈣結晶的形成並延遲磷灰石結晶凝聚,預防其溶解。在細胞水平上,二磷酸鹽抑制骨吸收,雖其作用機制不甚清楚,但已發現它改變破骨細胞形態、抑制破骨細胞活性,並減少其數量,使骨轉換率降低。目前在臨牀應用的雙磷酸鹽有以下幾種類型:
(1)依替膦酸(羥乙膦酸二鈉,依膦、邦得林),爲第一代雙磷酸鹽,長期或大量應用可阻滯正常骨組織的礦化,使骨折發生的危險性增加。因此主張週期性使用,並同時補充鈣劑。依替膦酸(依膦)的用法爲每天早飯前1小時服2片(每片200mg),以一杯溫開水吞下,或1片,每天兩次口服,連服14天后停藥,同時每天晚上口服鈣劑1片(500~600mg鈣),連服3個月。可重複2~4個療程。
(2)雙氯膦酸二二鈉(骨膦),間斷用藥,口服400mg/d,應用1個月,停藥2個月。
(3)阿侖膦酸鈉(Alendronate,福善美、天可、固邦),10mg/片,口服,1次/d或隔天一次。需空腹時服用,並需同時飲一滿杯水約200ml,不得同時飲用牛奶或其他含鈣飲料,並需保持直立姿勢,以防止藥物對食管的刺激。需按上方法服藥半小時後,纔可喫早飯,飲用其他飲料或藥物。阿侖膦酸鈉是新一代的雙磷酸鹽,通過側鏈基團的改變,不但消除了阻滯正常骨組織礦化之缺陷,而且抑制骨吸收的強度也大大增加。這些藥物,一旦吸收,可迅速分佈於骨組織,尤其是在松質骨最具代謝活性的骨表面有更高的藥物濃度。在血循環中的半衰期很短,約2h,但在骨組織中存留的半衰期很久,達數年,可強有力的抑制骨質的吸收。骨轉換率下降,最終導致骨量增加,骨折的發生率下降。一項對447名絕經婦女應用阿侖膦酸鈉(福善美)治療的經驗證實在腰椎、股骨頸及大轉子骨密度增加了1%~4%,全身骨密度增加了0.3%~1.0%。5mg,10mg,20mg 3種不同劑量的阿侖膦酸鈉(福善美)所進行的3年的研究證實,在治療期間骨密度增長,與5mg,20mg劑量相比較,10mg劑量組骨密度增加最明顯。5mg阿侖膦酸鈉(福善美)劑量已經被美國FDA批准用於預防骨質疏鬆。我國孟迅吾等對81例原發性骨質疏鬆症所進行的多中心開放研究,患者每天口服阿侖膦酸鈉(福善美)10mg和元素鈣500mg,結果腰椎2~4骨密度於治療3個月、6個月和12個月均較治療前有非常明顯的升高,分別爲2.8%,4.1%和6.3%,髖部骨密度在3,6,12個月也有顯著升高,以大轉子最爲顯著,升高2.6%~2.9%,其次爲股骨頸和Wards三角。
雙磷酸鹽的主要副作用爲消化道反應,可有噁心、嘔吐、腹瀉等,有消化道疾病者需慎用。需注意使用方法,以減少對胃腸道的刺激。
18.6 降鈣素(CT)
降鈣素(CT)是由甲狀腺濾泡旁細胞(C細胞)分泌的,由32個氨基酸組成的多肽,是調節鈣與骨代謝的激素之一。主要作用於骨和腎,抑制PTH、維生素D等引起的骨吸收因子。降鈣素(CT)對骨的作用,其一是直接抑制骨鹽溶解,使原始細胞轉變成破骨細胞的過程受到抑制,並加速破骨細胞向成骨細胞的轉化,使溶解過程減弱。其二是拮抗血鈣上升。血鈣較高時,降鈣素(CT)分泌增加,血鈣降低時,降鈣素(CT)分泌減少。此作用對維持生理骨量有重要意義。其三,降鈣素(CT)可拮抗PTH的促進骨鈣釋放入血液的作用。降鈣素(CT)具有鎮痛作用,其機制可能與改善鈣代謝、中樞性鎮痛作用及對肌肉收縮功能的作用有關。
降鈣素有鰻魚降鈣素(益鈣寧)和鮭魚降鈣素(密鈣息)兩種藥物。與破骨細胞膜表面受體結合,激活腺苷酸環化酶致CAMP升高,並激活磷脂肌肌醇系統致胞漿遊離鈣升高,兩種效應抑制破骨細胞吸收功能,具有增加骨量和明顯鎮痛作用。降鈣素(益鈣寧)每支10U、20U,用法爲10U每週2次或者20U每週1次肌內注射。降鈣素(密鈣息)每支50U,一天或隔天注射1次,持續2周,以後隔2天注射一次,持續3個月,每3個月爲一週期,用2~4個週期,即可提高骨量。降鈣素(密鈣息)也有鼻噴劑,50或100U/噴,一般用100U/次。
主要副作用爲頭昏、心慌、面部潮紅、噁心等不適。有過敏體質者、支氣管哮喘史者慎用。
18.7 選擇性雌激素受體調節劑(SERM)
SERM是一類人工合成的類似雌激素的化合物,它們選擇性作用於不同組織的雌激素受體,分別產生類雌激素或抗雌激素作用。對SERM的研究提示,作用於骨的雌激素受體亦能發揮類似雌激素樣作用。Richard發現接受他莫昔芬(三苯氧胺)治療兩年後的絕經後乳腺癌病人,腰椎骨密度每年平均增長0.61%,而對照組每年減少1.00%,二者有顯著差異。對切除卵巢的老年鼠及成長期鼠,他莫昔芬(三苯氧胺)、雷洛昔芬等同樣具有維持骨量、減少骨丟失的作用,但也有作者認爲SERM對骨作用的影響與雌激素水平有關。他莫昔芬(TAM)用於健康絕經前婦女,可使腰椎和髖部骨量進行性降低。表明在絕經前較高的雌激素水平時,他莫昔芬(TAM)對骨代謝的淨效應爲抗雌激素性的,而在絕經後內源性雌激素水平低下時,他莫昔芬(TAM)才表現出固有的對骨組織的雌激素樣作用。這可能與不同雌激素濃度下,雌激素受體的敏感性有關。雷洛昔芬與他莫昔芬(三苯氧胺)對骨量及血脂均有較好的影響,但在他莫昔芬(三苯氧胺)的臨牀研究中有引起子宮內膜增生,甚至誘發子宮內膜癌的報道。動物實驗發現大劑量他莫昔芬(三苯氧胺)可誘發大鼠肝癌,故雷洛昔芬的臨牀應用前景更爲看好。他莫昔芬(三苯氧胺)劑量爲10mg,口服2次/d,雷洛昔芬劑量爲60mg/d口服。
18.8 依普拉封
依普拉封是20世紀60年代後期在匈牙利合成的一種異黃酮衍生物,爲7-異丙氧基異黃酮。屬於植物雌激素類的一種。它在動物和人體中均沒有雌激素活性,但能增加雌激素的活性。在20世紀70年代初通過給小鼠、雞和羊口服依普拉芬天然合成衍生物,發現它能增加骨中的總鈣量,因而首次提出這類物質可作爲藥物治療骨質疏鬆。
對依普拉封的一些基礎研究證實可通過增加成骨細胞數量而增加骨形成,並可抑制骨吸收。依普拉芬對骨吸收抑制的機制與抑制前破骨細胞的募集和分化有關,而且這種抑制可通過降低成骨細胞對PTH反應而間接調節。
依普拉封對骨質疏鬆的治療作用與雌激素相似,但應用依普拉封的絕經後婦女,血清促性腺激素、雌激素或泌乳素水平無變化。爲了解依普拉封與雌激素受體間可能的相互作用,對人前破骨細胞系FLG29.1和人乳腺癌細胞系MCF7進行了研究。研究發現雌二醇和其他類固醇物質不能替代[3H]標記的依普拉封與FLG29.1細胞結合。同樣依普拉封也不能替代[3H]標記的雌二醇與MCF7細胞相結合。代謝產物預保溫後,雌激素與FLG29.1細胞的結合增加。依普拉封及其代謝產物不能引起FLG29.1雌激素受體相關基因的表達,也不引起MCF7對信息基因(CAT)和雌激素反應成分的影響。
上述結論提示,依普拉封作用於破骨細胞前體,而不是雌激素受體相互作用的調節。有關依普拉封的類雌激素作用及與雌激素受體結合的部位、直接或間接的作用等問題尚有爭議,還需在分子水平作進一步的研究。
劑量爲每天口服600mg,分3次給藥。不良反應主要是胃腸道反應,發生率在10%~16.1%。極少數患者出現可逆性白細胞減少,停藥後可恢復正常。
18.9 氟製劑
氟是骨和牙齒生長發育必需的微量元素,對骨有特殊的親和力,在骨質中取代羥磷灰石上的OH-,形成的氟磷灰石能拮抗破骨細胞的溶骨作用,並刺激成骨細胞的活性,促進骨形成,尤其增加松質骨的形成。應用氟化物時,必須配用足夠的鈣劑,才能使新骨轉變爲成熟骨。單氟磷酸谷酰胺與鈣劑合製成的特樂定嚼片(每片含氟元素5mg,鈣元素150mg)目前已用於臨牀,3~4片/d,口服,有消化道刺激的不適反應。
18.10 甲狀旁腺素(PTH)
小劑量間隙皮下注射PTH在動物實驗中有成骨作用,可使骨量增加,並提高抗骨折能力,目前臨牀應用資料較少,還需要臨牀進一步觀察研究。
20 絕經後骨質疏鬆的預防
絕經後隨年齡增加,骨密度將漸進性減少,並使骨質疏鬆症的風險及骨折的危險度劇增。預防的主要目標是在婦女的整個生命過程中控制骨質疏鬆的危險因素(圖3)。
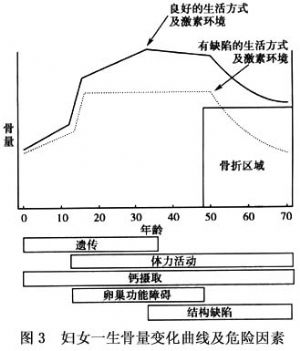
20.1 青年至老年期避免骨質疏鬆症的高危因素
這些因素包括大量的吸菸、酗酒、久坐的生活方式、厭食及服用某些藥物(如皮質激素類、肝素和某些抗癲癇藥物等)。應注重戶外活動,日照、營養、適度負重鍛鍊並防止跌倒。
20.2 青年期注意鈣的補充
這種方法與有規律的,適量的運動相結合,可使女性獲得較理想的峯值骨量。
20.3 絕經後防止雌激素喪失
在絕經後第1個5~10年使用激素替代療法預防骨質疏鬆症的效果是肯定的。然而,由於激素替代療法有其適應證與禁忌證,應針對不同個體在醫生監護下使用纔是安全的。
20.4 補充鈣劑和維生素D,聯合應用抗骨吸收藥物
在老年期補充鈣劑和維生素D可以部分防止骨量丟失和骨質疏鬆性骨折,但是如果聯合應用抗骨吸收藥物(雌激素、降鈣素、雙磷酸鹽等)將起到顯著的治療作用。
雖然有些危險因素如早絕經和骨質疏鬆家族史等是無法改變的,但通過以上干預措施確實可以使高危人羣獲益,減少骨質疏鬆症及骨折發病率。
20.5 防止老年人摔倒
有人報道每年約有1/3以上≥65歲的老年人摔倒,其中半數是再次發生的摔倒。10次摔倒中約有1次引起嚴重的損傷,如骨盆骨折,其他部位骨折,硬腦膜下血腫、其他部位的嚴重軟組織損傷及頭部損傷。老年人骨質疏鬆性骨折治療較爲困難,如長期臥牀則使血流緩慢、肺及氣管的分泌物排出不暢易至心血管疾病及肺部感染,這將使老年患者死亡率上升。因此防止老年人摔倒,避免骨折的發生,可以有效地改善老年人的生活質量。
與摔倒相關的因素有關節炎病;抑鬱狀態;靜態平穩位(orthostasis);認知功能、視力、平衡、步態或肌力方面的障礙;使用多種藥物等。與摔倒危險增加相關的藥物有5-羥色胺再攝取抑制劑、三環類抗抑鬱藥、精神安定劑、利眠寧、抗驚厥藥及一些抗心率失常藥。
醫生應瞭解患者有否摔倒的病史,並找出引起摔倒的危險因素並避免其發生。對家中的危險因素評估後應向病人提出針對性的建議,最常建議的措施是撤掉鬆動的地毯,改用較安全的鞋子(能包裹足部、低跟、薄底的大小合適的鞋),使用不滑的浴墊,在晚上使用照明裝置和在樓梯上加裝欄杆。這些行之有效的措施可使老人摔倒的危險降低約20%。
在專業人員指導下的平衡和步態訓練以及增強肌力的鍛鍊,逐步減少及停止使用精神藥物也與摔倒發生率下降有關。對於有眼病、暈厥、心律失常患者均應轉眼科、心臟科醫師處就診以查明原因,針對性治療,防止摔倒的發生。