b型流感嗜血杆菌结合疫苗药典标准
品名
中文名
b型流感嗜血杆菌结合疫苗
汉语拼音
b Xing Liuganshixueganjun Jiehe Yimiao
英文名
Haemophilus Influenzae Type b Conjugate Vaccine
定义、组成及用途
本品系用纯化的b型流感嗜血杆菌(Hib)荚膜多糖抗原,通过己二酰肼与破伤风类毒素蛋白共价结合制成。用于预防b型流感嗜血杆菌引起儿童的感染性疾病,如脑膜炎、肺炎等。
1 基本要求
生产和检定用设施、原材料及辅料、水、器具、动物等应符合“凡例”的有关要求。
2 制造
2.1 菌种
生产用菌种应符合“生物制品生产检定用菌毒种管理规程”的有关规定。
2.1.1 名称及来源
采用b型流感嗜血杆菌CMCC 58547或CMCC 58534株。
2.1.2 种子批的建立
应符合“生物制品生产检定用菌毒种管理规程”的规定。
2.1.3 种子批的传代
主种子批启开后传代次数不超过5代,工作种子批启开后至接种发酵罐培养传代次数不得超过5代。
2.1.4 种子批的检定
检定菌种可用含羊血的巧克力培养基或Hib综合培养基。
2.1.4.1 培养特性
菌种在普通营养琼脂培养基上不生长,在含羊血的巧克力培养基或在Hib综合琼脂培养基上生长,生长需要X因子(氯化血红素)、V因子(β辅酶A);卫星试验阳性,菌落呈灰白色、半透明、光滑凸起,湿润,边缘规则。
2.1.4.2 染色镜检
应为革兰氏阴性短小杆菌,有荚膜,有时连成线状,亦可有单个阴性球菌。
2.1.4.3 生化反应
发酵葡萄糖、木糖、半乳糖,产酸不产气。不发酵蔗糖、乳糖和果糖(2010年版药典三部附录XIV)。赖氨酸脱羧酶反应呈阴性。
2.1.4.4 血清学试验
将在35~37℃培养的菌苔,与Hib免疫血清进行玻片凝集试验,应有强凝集反应。
2.1.5 种子批的保存
种子批应冻干保存于8℃以下。
2.2 原液
2.2.1 生产用种子
启开工作种子批菌种,一经适当传代检查培养特性和染色镜检后接种在液体或固体Hib综合培养基上,制备数量适宜的生产用种子。
2.2.2 生产用培养基
采用Hib综合培养基。
2.2.3 培养
采用培养罐液体培养,在培养过程中取样进行纯菌试验、涂片革兰氏染色镜检,如发现污染杂菌,应废弃。
2.2.4 收获及杀菌
于对数生长期的后期或静止期的前期收获,取样进行菌液浓度测定及纯菌检查,然后于培养物中加入适宜浓度的甲醛溶液或脱氧胆酸钠溶液杀菌,以确保杀菌完全及不损伤Hib荚膜多糖为宜。
2.2.5 多糖提取和纯化
2.2.5.1 去核酸
将已杀菌的培养物,离心去菌体后收集上清液,采用十六烷基三甲基溴化铵沉淀收集复合多糖。
2.2.5.2 沉淀多糖
乙醇沉淀收集粗制多糖,或超滤浓缩后乙醇沉淀,取上清液,然后加入适宜浓度的乙醇溶液沉淀多糖,并依次用无水乙醇、丙酮洗涤沉淀物,干燥后即为粗制多糖,-20℃或以下保存。
2.2.5.3 多糖纯化
将粗制多糖溶解于1/10饱和醋酸钠溶液中,然后按适当比例用冷酚溶液重复抽提数次。收集上清液,并透析或超滤脱酚,再加乙醇至最终浓度为60%~80%,离心后收集沉淀物,或超滤浓缩后乙醇沉淀,取上清液,然后加入60%~80%的乙醇溶液沉淀多糖,依次用无水乙醇、丙酮洗涤,真空干燥,所得固体即为精制多糖。
2.2.5.4 多糖检定
按3.1项进行。
2.2.5.5 保存及有效期
保存于-20℃或以下,保存时间按批准的执行。
2.2.6 多糖衍生
2.2.6.1
将精制多糖溶解后,按适宜比例加入溴化氰进行活化,然后向反应液中加入适宜浓度的己二酰肼溶液,反应过夜。再将反应液超滤或透析。可冻干收集固体衍生物。
2.2.6.2 多糖衍生物检定
按3.2项进行。
2.2.6.3 保存及有效期
保存于-20℃或以下,保存时间不超过30天。
2.2.7 载体蛋白
载体蛋白为破伤风类毒素。破伤风类毒素原液制造和检定应符合“吸附破伤风疫苗”2.1~2.2项规定。
可采用柱色谱法或其他经批准的方法对破伤风类毒素原液进一步纯化,并配制至适宜浓度。
2.2.8 多糖蛋白结合物的制备
2.2.8.1 结合
多糖衍生物与破伤风类毒素蛋白等量混合,加入碳二亚胺( EDAC)进行反应,然后透析或超滤透析。
2.2.8.2 结合物纯化
结合物用柱色谱纯化,收集Vo附近的洗脱液,合并各次色谱收获的洗脱液即为纯化的结合物,除菌过滤后,即为结合物原液。
2.2.9 原液检定
按3.3项检定。
2.2.10 保存及有效期
保存于2~8℃,保存时间不超过6个月。
2.3 半成品
2.3.1 配制
用氯化钠注射液稀释多糖蛋白结合物原液,每1ml疫苗溶液含多糖应不低于20μg。
2.3.2 半成品检定
按3.4项进行。
2.4 成品
2.4.1 分批
应符合“生物制品分批规程”规定。
2.4.2 分装
应符合“生物制品分装和冻干规程”规定。
2.4.3 规格
每瓶0.5ml。每1次人用剂量0.5ml,含多糖10μg。
2.4.4 包装
应符合“生物制品包装规程”规定。
3 检定
3.1 多糖检定
3.1.1 鉴别试验
采用免疫双扩散法(2010年版药典三部附录Ⅷ C),本品应与b型流感嗜血杆菌免疫血清形成明显沉淀线。
3.1.2 化学检定
3.1.2.1 固体总量
依法测定(2010年版药典三部附录Ⅶ M)。
3.1.2.2 核糖含量
以D-核糖为对照,应为320~410mg/g(2010年版药典三部附录Ⅷ J)。
3.1.2.3 磷含量
应为68~90mg/g(2010年版药典三部附录Ⅶ A)。
3.1.2.4 蛋白质含量
应小于10mg/g(2010年版药典三部附录Ⅵ B第二法)。
3.1.2.5 核酸含量
应小于10mg/g,核酸在波长260nm处的吸收系数( 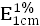 )为200(2010年版药典三部附录Ⅱ A)。
)为200(2010年版药典三部附录Ⅱ A)。
3.1.2.6 多糖分子大小测定
采用琼脂糖CL-4B凝胶柱(1.6cm×100cm)测定,KD≤0.5的多糖回收率应不低于50%(2010年版药典三部附录Ⅷ G)。
3.1.3 细菌内毒素检查
应不高于25EU/μg(2010年版药典三部附录Ⅻ E)。
3.2 多糖衍生物检定
3.2.1 己二酰肼含量
应为16~45μg/mg(2010年版药典三部附录Ⅷ K)。
3.2.2 氰化物残留量
应不高于10ng/mg(2010年版药典三部附录Ⅵ X)。
3.3 结合物原液检定
3.3.1 鉴别试验
采用免疫双扩散法(2010年版药典三部附录Ⅷ C),本品应与b型流感嗜血杆菌免疫血清及破伤风类毒素免疫血清形成明显沉淀线。
3.3.2 化学检定
3.3.2.1 多糖含量
以D-核糖为对照,按核糖含量计算结合物中多糖含量,应不低于28μg/ml(2010年版药典三部附录Ⅷ J)。
3.3.2.2 蛋白质含量
应不低于48μg/ml(2010年版药典三部附录Ⅵ B第二法)。
3.3.2.3 多糖与蛋白质的比值
按3.3.2.1和3.3.2.2测定结果计算,应为0.30~0.59。
3.3.2.4 高分子结合物含量
高分子结合物应为80%~100%或游离多糖≤20%(2010年版药典三部附录Ⅷ L)。
3.3.2.5 多糖分子大小测定
采用琼脂糖CL-4B凝胶柱(1.6cm×100cm)测定,KD值应不高于0.20,KD值小于0.20的洗脱液回收率应不低于60%(2010年版药典三部附录Ⅷ G)。
3.3.2.6 EDAC残留量
采用N.Wilchek方法测定,EDAC残留量应低于10μmol/L(2010年版药典三部附录Ⅵ Y)。
3.3.3 无菌检查
依法检查(2010年版药典三部附录Ⅻ A),应符合规定。
3.3.4 细菌内毒素检查
应不高于5FU/μg(2010年版药典三部附录Ⅻ E)。
3.4 半成品检定
无菌检查
依法检查(2010年版药典三部附录Ⅻ A),应符合规定。
3.5 成品检定
3.5.1 鉴别试验
采用免疫双扩散法(2010年版药典三部附录Ⅷ C),应与b型流感嗜血杆菌免疫血清及破伤风类毒素免疫血清形成明显沉淀线。
3.5.2 物理检查
3.5.2.1 外观检查
应为无色透明液体,无异物。
3.5.2.2 装量
依法检查(2010年版药典三部附录Ⅰ A),应不低于标示量。
3.5.3 化学检定
3.5.3.1 pH值
应为5.0~7.0(2010年版药典三部附录Ⅴ A)。
3.5.3.2 氯化钠含量
应为7.5~9.5/L(2010年版药典三部附录Ⅶ G)。
3.5.3.3 多糖含量
以D-核糖为对照,按核糖含量计算供试品中多糖含量,每1次人用剂量应为10~15μg(2010年版药典三部附录Ⅷ J)。
3.5.3.4 高分子结合物含量
高分子结合物应为80%~100%或游离多糖≤20%(2010年版药典三部附录Ⅷ L)。
3.5.3.5 多糖分子大小测定
采用琼脂糖CL-4B凝胶柱(1.6cm×100cm),KD值小于0.2的洗脱液回收率应大予60%(2010年版药典三部附录Ⅷ G)。
3.5.4 效力试验
每批疫苗皮下注射体重12~14g NIH(或BALb/c)小鼠10只,另取同批小鼠10只作为对照,注射0.85%氯化钠溶液。于第1、14天皮下注射两次,每次注射剂量为含2.5μg多糖的Hib结合疫苗,于第21~28天经眼眶后静脉采血,以ELISA法测定抗Hib IgG抗体,以0.85%氯化钠溶液对照组小鼠血清的A值求出Cutoff值,疫苗组应有80%以上小鼠的血清抗Hib IgG抗体水平高于Cutoff值。
3.5.5 无菌检查
依法检查(2010年版药典三部附录Ⅻ A),应符合规定。
3.5.6 热原检查
依法检查(2010年版药典三部附录Ⅻ D),注射剂量按家兔体重每1kg注射1.0μg多糖,应符合规定。
3.5.7 异常毒性检查
依法检查(2010年版药典三部附录Ⅻ F),应符合规定。
3.5.8 细菌内毒素检查
每1次人用剂量应不高于25EU(2010年版药典三部附录Ⅻ E)。
4 保存、运输及有效期
于2~8℃保存和运输。自生产之日起,有效期为24个月。
5 使用说明
应符合“生物制品包装规程”规定和批准的内容。
b型流感嗜血杆菌结合疫苗使用说明
【药品名称】
通用名称:b型流感嗜血杆菌结合疫苗
英文名称:Haemophilus Influenzae Type b Conjugate Vaccine
汉语拼音:b Xing Liuganshixueganjun Jiehe Yimiao
【成分和性状】
本品系用纯化的b型流感嗜血杆菌荚膜多糖与破伤风类毒素共价结合而成。为无色透明液体,含防腐剂。
有效成分:b型流感嗜血杆菌荚膜多糖。
辅料:应列出全部批准的辅料成分。
【接种对象】
2或3月龄婴儿~5周岁儿童。
【作用与用途】
本疫苗接种后,可使机体产生体液免疫应答。用于预防由b型流感嗜血杆菌引起的侵袭性感染(包括脑膜炎、肺炎、败血症、蜂窝组织炎、关节炎、会厌炎等)。
【规格】
每瓶为0.5ml,每1次人用剂量为0.5ml,含纯化b型流感嗜血杆菌荚膜多糖应不低于10μg.
【免疫程序和剂量】
臀部外上方1/4处或上臂外侧三角肌肌内注射。
自2 (3)月龄开始,每隔1个月或2个月接种1次(0.5ml),共3次,在18个月时进行加强接种1次;6~12月龄儿童,每隔1个月或2个月注射1次(0.5ml),共2次,在18个月时进行加强接种1次;1~5周岁儿童,仅需注射1次(0.5ml)。
【不良反应】
注射后一般反应轻微,接种部位可出现轻微红肿、硬结、压痛,偶有局部瘙痒感,一般不需特殊处理,即自行消退。必要时可对症治疗。
全身反应:主要为发热反应(多在38.5℃以下),偶有烦躁、嗜睡、呕吐、腹泻、食欲不振,偶见非典型的皮疹,一般可自行缓解。
【禁忌】
(1)患急性疾病、严重慢性疾病、慢性疾病的急性发作期和发热者。
(2)已知对该疫苗的任何成分过敏,特别对破伤风类毒素过敏者。
(3)严重心脏疾病、高血压,患肝脏疾病、肾脏疾病者。
【注意事项】
(1)以下情况者慎用:家族和个人有惊厥史者、患慢性疾病者、有癫痫史者、过敏体质者。
(2)使用前应充分摇匀,如出现摇不散的凝块,异物,疫苗瓶有裂纹、标签不清或过期失效者,均不得使用。
(3)接受免疫抑制治疗或免疫缺陷患者注射本疫苗可能影响疫苗的免疫效果。
(4)应备有肾上腺素等药物,以备偶有发生严重过敏反应时急救用。接受注射者在注射后应在现场观察至少30分钟。
(5)本疫苗如与其他疫苗同时接种,应在不同的部位注射。
(6)在任何情况下,疫苗中的破伤风类毒素不能代替常规破伤风类毒素的免疫接种。
(7)严禁冻结。
【贮藏】
于2~8℃避光保存和运输。
【包装】
【有效期】
24个月。
【执行标准】
【批准文号】
【生产企业】
企业名称:
生产地址:
邮政编码:
电话号码:
传真号码:
网 址:
版本
《中华人民共和国药典》2010年版